51直播 新闻
Military Medical Research丨北京大学冼勋德/董尔丹/王宇辉/赵东宇联合发现马达蛋白KIF13B是合并治疗MAFLD和ASCVD的新靶点
51直播
近日,北京大学心血管研究所冼勋德课题组在期刊Military Medical Research杂志上发表了题为Motor protein KIF13B orchestrates hepatic metabolism to prevent metabolic dysfunction-associated fatty liver disease的文章。该研究聚焦于一种鲜为人知但极具潜力的靶点——马达蛋白KIF13B,首次系统性地揭示了其在调控肝脏脂质代谢和线粒体功能中的重要作用以及与MAFLD之间的潜在关联。

代谢障碍相关脂肪性肝病(MAFLD)是一种高度复杂的全球性健康问题,目前影响着超过四分之一的世界人口,每年导致约4%的全球死亡率。作为一种代谢紊乱疾病,MAFLD以肝脏脂肪过度堆积为特征,通常与肥胖、糖尿病、高脂血症等代谢异常密切相关。其进程从代谢相关脂肪性肝(MAFL)开始,逐渐发展为更严重的代谢相关脂肪性肝炎(MASH),并可能进一步导致肝纤维化、肝硬化、肝细胞癌等严重并发症,甚至是全身性的代谢紊乱。尽管近年来治疗MAFLD的研究取得了一定进展,并且美国食品药品监督管理局(FDA)新近批准了一款新型甲状腺激素受体激动剂用于治疗非肝硬化性MASH,但由于MAFLD的病因复杂多样、病理机制高度异质化,目前尚缺乏全面有效的治疗方案。因此,寻找新的治疗靶点并开发创新疗法已成为解决这一重大公共健康问题的迫切需求。
研究团队通过对患者样本以及多种动物模型的联合分析发现,KIF13B在MAFLD患者及小鼠模型中的表达水平显著降低,其缺失会导致肝脏脂质代谢的显著紊乱和线粒体功能障碍。进一步的实验表明,无论是在全身性还是肝脏特异性敲除Kif13b基因的小鼠和仓鼠模型中,均观察到自发性肝脂肪变性,该病变在高脂饮食的诱导下进一步加剧。此外,慢病毒介导的Kif13b基因过表达实验显示,该基因的恢复可以显著抑制由缺乏甲硫氨酸和胆碱的饮食诱导的小鼠MASH的发生,为潜在治疗MAFLD提供了有力的证据。
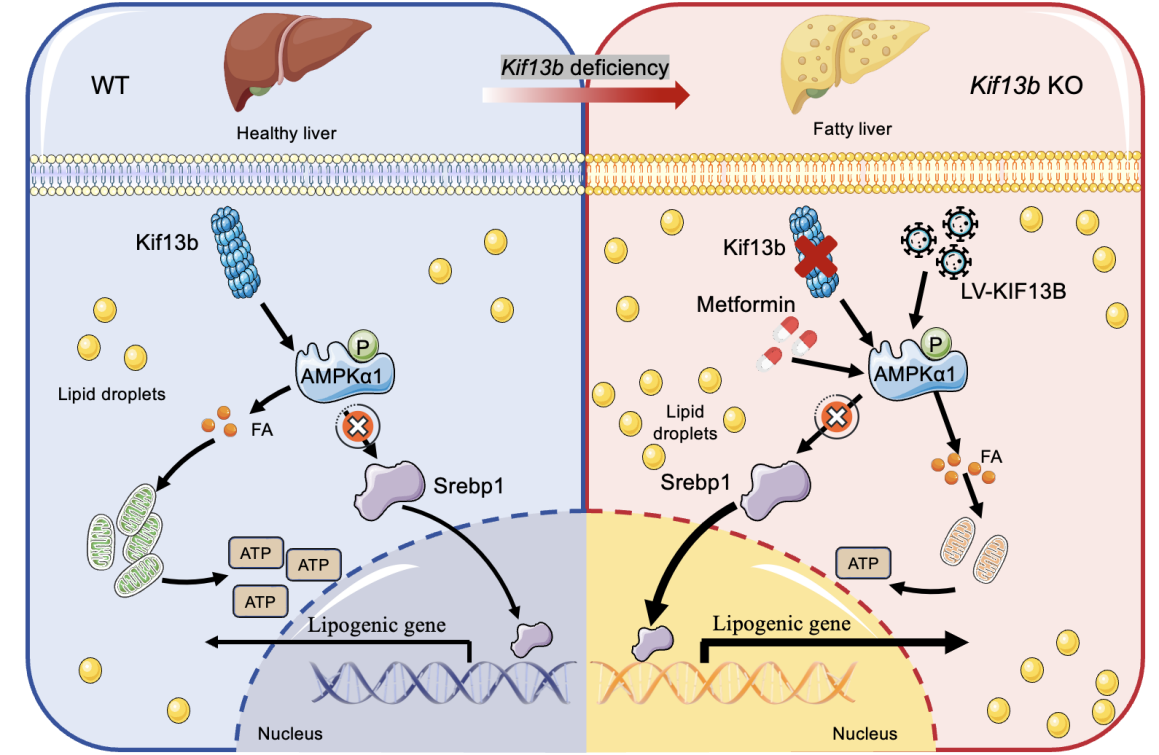
从分子机制上看,本研究揭示了KIF13B通过与AMP激活的蛋白激酶α1(AMPKα1)相互作用来调控其磷酸化水平,从而维持线粒体的稳态功能。具体而言,KIF13B能够增强线粒体的氧化磷酸化能力,抑制与脂质生成密切相关的Srebp1c基因的活性,避免脂质过度生成和堆积。而这一保护性作用的显著特点在于,其在增强线粒体功能的同时避免了传统治疗方法可能引发的氧化应激和相关毒性风险,具有明显的安全性优势。此外,研究还发现,在MAFLD背景下,Kif13b基因缺失会进一步加速动脉粥样硬化的进展,提示其在保护心血管系统中的潜在重要作用。
本研究的创新之处在于,首次明确了KIF13B在调控肝脏脂质代谢和线粒体功能中的核心作用,并将其确立为一个潜在的治疗靶点。相比现有的治疗方法,KIF13B靶点治疗不仅可以通过改善肝脏线粒体代谢功能,减轻脂肪堆积并阻止疾病进展,还具有显著的安全性优势。这为未来开发针对MAFLD的精准治疗药物提供了全新的科学依据。
总而言之,MAFLD的治疗是一个高度复杂且未被充分解决的医学挑战。本研究通过对KIF13B的深入探索,不仅在疾病机制上取得了重要突破,还为临床治疗提供了潜在的新思路。这一发现为应对全球MAFLD高发和高致死率问题带来了希望,同时也为探索更广泛的代谢性疾病治疗奠定了重要基础。未来,针对KIF13B的进一步研究和药物开发可能将为全球范围内数百万患者带来福音。
北京大学心血管研究所冼勋德研究员、董尔丹院士、王宇辉副研究员、51直播 医学生物信息学系赵东宇研究员为本文共同通讯作者。博士后苗国琳、博士生张文茜、徐一童和刘一冉为本文共同第一作者。本研究得到心血管所黄薇副教授与中国医学科51直播 实验动物研究所马元武研究员、北京大学未来技术51直播 赵扬研究员的帮助,受到国家自然科学基金委、北京市自然科学基金委和血管稳态与重构全国重点实验室的大力支持。
原文链接:
//mmrjournal.biomedcentral.com/articles/10.1186/s40779-025-00594-3

